Регистрация масс-спектров ионизации электрораспылением (ИЭР, ESI).
МС
Масс-спектрометрия
Масс-спектрометр тандемный ULTRAFLEX III TOF/TOF «Bruker», Германия
Регистрация масс-спектров матрично-активированной лазерной десорбции/ионизации (МАЛДИ, MALDI).
Хромато-масс-спектрометр высокого разрешения с двойной фокусировкой DFS «Thermo Fisher Scientific», США
Измерение содержания различных веществ в пробах веществ и материалов, растворах и т.д. Регистрация масс-спектров при электронной и химической ионизации. Определение точных масс для неизвестных органических соединений.
Масс-спектрометрия
Требования к образцам, предоставляемым на типовой анализ, пример оформления экспериментальной части при публикации результатов
Общие сведения и общие требования
Типовой анализ выполняется по стандартным методикам без проведения каких-либо дополнительных экспериментов, подбора условий и т.п. Интерпретация полученных данных операторами не производится. На каждый образец (серию образцов) должна быть оформлена заявка, соответствующая требуемому анализу.
Выполнение работ, не подпадающих под типовой анализ, – предполагающих подбор условий и обсуждение результатов эксперимента, предусматривает участие научных сотрудников для решения поставленной задачи, оговаривается с заведующим лабораторией и оформляется заявкой на выполнение научных исследований.
Виалы (эппендорфы и т.д.) должны иметь герметично закрывающиеся крышки (не допускающих самопроизвольное открывание). В случае сильнопахнущих образцов место закручивания крышки должно обязательно изолироваться герметизирующей пленкой (парафилм). Количество образца должно быть таковым, чтобы оператор мог без особых усилий отобрать образец на анализ. В случае жидких образцов и растворов образцов виалу предпочтительно заполнять на 1/2–2/3 объема.
Виалы (эппендорфы, бюксы и т.д.) должны иметь этикетку с шифром образца. Допускается делать надпись на виале маркером и поверх приклеивать прозрачную ленту (заказчик должен позаботиться о том, чтобы надпись не была случайно смыта водными или органическими растворителями).
Шифр образца должен состоять из букв латинского алфавита и арабских цифр без каких-либо других знаков (не допускается использование точки, тире, знака подчеркивания и т.п.), всего не более восьми символов. Предпочтительно чтобы шифр соответствовал формату: VFIO###, где V – код вида анализа, F, I, O – первые буквы фамилии, имени и отчества заявителя (только буквами латинского алфавита), ### – номер пробы.
Коды видов анализа:
| G | Газовая хромато-масс-спектрометрия (ЭИ,EI) |
| M | Масс-спектрометрия МАЛДИ (MALDI) |
| E | Масс-спектрометрия с ионизацией электрораспылением (ИЭР, ESI) |
Место и время предоставления образцов по видам анализа:
Газовая хромато-масс-спектрометрия, DFS – к. 124 (9.00–11.00)
Mасс-спектрометрия MALDI – к. 115 (9.00–11.00)
Mасс-спектрометрия ESI – к. 115 (9.00–11.00)
С вопросами и консультациями по поводу подготовки образцов к типовому анализу и результатов анализа обращаться только в указанное время!
Последняя пятница каждого месяца является санитарным днем, – прием и анализ образцов не производится.
Типовой анализ предоставленных образцов выполняется в течение 1-3 дней. Анализ образцов может задерживаться из-за неисправности или технического обслуживания оборудования, а также при высокой загрузке оборудования и сотрудников лаборатории, в том числе в связи с проведением длительных исследовательских экспериментов.
График загрузки оборудования доступен для просмотра по ссылке https://docs.google.com/spreadsheets/d/1Msy9PBA1UNm_9AAZj8lyfyG0ZwfedHn6UY48OwBxc_c/edit#gid=1942926870
Предоставленные образцы в случае их невостребованности в течение двух недель после проведения анализа утилизируются.
Публикация результатов
В случае опубликования результатов, полученных на оборудовании ЦКП, заказчик обязан указывать в благодарностях ссылку на ЦКП-САЦ ФИЦ КазНЦ РАН, например:
На русском языке: 1) «Авторы благодарят сотрудников Распределенного коллективного спектро-аналитического Цента изучения строения, состава и свойств веществ и материалов Федерального государственного бюджетного учреждения науки «Федерального исследовательского центра «Казанского научного центра Российской академии наук» за проведенные исследования и помощь в обсуждении результатов»,
2) «Авторы благодарят ЦКП-САЦ ФИЦ КазНЦ РАН за проведенные исследования».
На английском языке: 1) «The authors are grateful to the staff of Assigned Spectral-Analytical Center of Shared Facilities for Study of Structure, Composition and Properties of Substances and Materials of Federal Research Center of Kazan Scientific Center of Russian Academy of Sciences» for their research and assistance in discussing the results»,
2) «The authors gratefully acknowledge the CSF-SAC FRC KSC RAS for providing necessary facilities to carry out this work».
Выбор метода масс-спектрометрического анализа (метода ионизации)
Газовая хромато-масс-спектрометрия
Подготовка образца для ГХ/МС анализа:
Образцы должны быть растворены в подходящем растворителе (предпочтительно использование таких растворителей как метанол, ацетонитрил, гексан, бензол, толуол, хлороформ) в концентрации 5-10 мг/мл. Раствор образца предоставляется в количестве 0,5-1,5 мл в виале (объемом 1,5-2 мл) с закручивающейся крышкой. Растворы образцов не должны содержать минеральных солей, кислот и оснований, а также полимеров и смол! Растворы образцов не должны иметь взвешенных частиц и мути (такие растворы к анализу допускаться не будут). Для анализа термолабильных, высокомолекулярных (ММ>800 Да), труднолетучих (Ткип > 250 °С и Тпл > 150 °С) соединений проведение ГХ/МС не целесообразно.
Пример оформления для ГХ/МС анализа:
Хромато-масс-спектрометрический анализ проводили на хромато-масс-спектрометре DFS Thermo Electron Corporation (США) производства «Shimadzu» (Япония). Температура интерфейса и источника ионов 250 °С. Колонка TG-5MS длиной 30 м, внутренний диаметр 0,25 мм, толщина пленки неподвижной фазы 0,25 мкм. Режим анализа: программирование температуры от 25 до 200 °С со скоростью 5 град/мин, газ-носитель – гелий (расход 2 мл/мин), деление потока при вводе проб 1:10, время отсечения растворителя 3 мин, температура испарителя 250 °С, объем дозируемой пробы 0,5 мкл. Данные были обработаны с помощью программы XCalibur.
На английском языке: Electron ionisation (EI) mass spectra were obtained using gas chromatomass spectrometry with DFS Thermo Electron Corporation (USA) instrument at electron ionization energy of 70 eV, temperature of the ion source of 250 °C. Capillary column TG-5MS with the length of 30 m and diameter of 0.25 mm was used. The chromatographic conditions were following: the flow rate of carrier gas (Helium) was 2 mL·min−1, injector temperature was 250 °C, initial thermostate temperature was 160 °C (1 min), heating rate was 20 deg·min−1, final thermostate temperature was 280 °C (15 min). The data treatment was performed using XCalibur software.
Mасс—спектрометрия МАЛДИ (MALDI)
Подготовка образца для МАЛДИ анализа:
Предоставляемые образцы должны быть растворены в подходящем растворителе в концентрации 1 мг/мл. Раствор образца предоставляется в количестве 0,5-1,5 мл в виале (объемом 1,5-2 мл) с закручивающейся крышкой или эппендорфе (с хорошо закрывающейся крышкой). Растворы образцов не должны содержать сильных кислот и оснований. Желательно предоставлять на анализ предварительно очищенные образцы (индивидуальные соединения), ввиду того, что наличие хорошо ионизирующихся примесей (иногда подавляющих сигнал целевого соединения) приводит к ошибочной интерпретации масс-спектров.
Пример оформления экспериментальной части при публикации результатов:
Масс-спектры МАЛДИ были получены на масс-спектрометре Ultraflex III TOF/TOF
(Bruker Daltonik GmbH, Германия), оснащенном лазером Nd:YAG (λ=355 нм, частота 100 Гц), в линейном режиме с регистрацией положительно заряженных ионов. Масс-спектр был получен с ускоряющим напряжением 25 кВ и временем задержки экстракции ионов 30 нс. Итоговый масс-спектр был сформирован за счет многократного облучения лазером кристалла (50 лазерных импульсов). Использовалась металлическая мишень MTP AnchorChipTM. На мишень последовательно наносили и упаривали 0,5 мкл 1% раствора матрицы в ацетонитриле и 0,5 мкл 0,1% раствора образца в метаноле. Данные были получены с помощью программы FlexControl (Bruker Daltonik GmbH, Германия) и обработаны с помощью программы FlexAnalysis 3.0 (Bruker Daltonik GmbH, Германия).
На английском языке: The MALDI mass spectra were recorded on an Ultraflex III TOF/TOF mass spectrometer (Bruker Daltonic GmbH, Bremen, Germany) operated in the linear mode with the registration of positively charged ions or negatively charged ions. A Nd:YAG laser (λ = 355 nm, repetition rate 100 Hz) was used. The mass spectrum was obtained with an accelerating voltage of 25 kV and an ion extraction delay time of 30 ns. The resulting mass spectrum was formed due to multiple laser irradiation of the crystal (50 shots). The metal target MTP AnchorChipTM was used. Portions (0.5 μl) of a 1% matrix solution in acetonitrile and of a 0.1% sample solution in methanol were consecutively applied onto the target and evaporated. 2,5-Dihydroxybenzoic acid (DHB) was used as a matrix. The polyethylene glycol was used to calibrate the mass scale of the device. The data was obtained using the FlexControl program (Bruker Daltonik GmbH, Germany) and processed using the FlexAnalysis 3.0 program (Bruker Daltonik GmbH, Germany).
Mасс-спектрометрия ИЭР (ESI)
Подготовка образца для ИЭР анализа:
Предоставляемые на масс-спектрометрический анализ образцы должны быть растворены в подходящем растворителе (предпочтительно использование таких растворителей как спирты, ацетонитрил, вода) в концентрации 1 мг/мл (дальнейшее разбавление образца производится оператором). Раствор образца предоставляется в количестве 0,5-1,5 мл в виале (объемом 1,5-2 мл) с закручивающейся крышкой или эппендорфе (с хорошо закрывающейся крышкой). Растворы образцов не должны содержать детергентов (ПЭГ и др.) подавляющих ионизацию аналита, а также сильных кислот и оснований. Желательно предоставлять на анализ образцы, представляющие собой предварительно очищенные (индивидуальные) соединения, ввиду того, что наличие хорошо ионизирующихся примесей (иногда подавляющих сигнал целевого соединения) приводит к ошибочной интерпретации масс-спектров. Растворы образцов не должны иметь взвешенных частиц и мути (такие растворы к анализу допускаться не будут)!
Пример оформления экспериментальной части при публикации результатов:
Масс-спектры ионизации электрораспылением (ИЭР) получены на масс-спектрометре AmazonX (Bruker Daltonik GmbH, Германия) с ионной ловушкой. Измерение проводилось в режиме регистрации положительных (и/или отрицательных) ионов в диапазоне m/z от 70 до 3000. Напряжение на капилляре распылителя составляло −3500 В. В качестве газа-осушителя использовался азот с температурой 250 °С и расходом 10 л∙мин-1. В качестве элюента использовали раствор состава метанол/вода (70:30, об.) со скоростью потока 0,2 мл/мин (хроматограф Agilent 1260, США). Анализируемый образец растворяли в метаноле до концентрации 10-6 г/л. Ввод образца в поток производился через инжектор Rheodyne 7725 (Rheodyne, США). Объем вкалываемой пробы 20 мкл. Для управления масс-спектрометром и сбора данных использовалось программное обеспечение TrapControl 7.0 (Bruker Daltonik GmbH, Германия). Данные обрабатывались с помощью программы DataAnalysis 4.0 SP4 (Bruker Daltonik GmbH, Германия).
На английском языке: The ESI MS measurements were performed using an AmazonX ion trap mass spectrometer (Bruker Daltonic GmbH, Germany) in positive (and/or negative) mode in the mass range of 70–3000. The capillary voltage was −3500 V, nitrogen drying gas – 10 L·min-1, desolvation temperature – 250 °С. An methanol/water solution (70:30) was used as a mobile phase at a flow rate of 0.2 mL/min by binary pump (Agilent 1260 chromatograph, USA). The sample was dissolved in methanol to a concentration of 10-6 g·L-1. The instrument was calibrated with a tuning mixture (Agilent G2431A, USA). For instrument control and data acquiring the TrapControl 7.0 software (Bruker Daltonik GmbH, Germany) was used. Data processing was performed by DataAnalysis 4.0 SP4 software (Bruker Daltonik GmbH, Germany).
Масс-спектрометрия
Рекомендуемая литература
- Сильверстейн Р., Вебстер Ф., Кимл Д. Спектрометрическая идентификация органических соединений. пер. с англ. – М.: БИНОМ. Лаборатория знаний, 2011. – 557 с.
- Казицына Л.А., Куплетская Н.Б. Применение УФ-, ИК-, ЯМР-спектроскопии в органической химии – М.: Высшая школа, 1971. – 264 с.
- Вилков Л.В., Пентин Ю.А. Физические методы исследования в химии. Структурные методы и оптическая спектроскопия – М.: Высшая школа, 1987. – 367 с.
- Смит А. Прикладная ИК-спектроскопия. Основы. Техника. Аналитическое применение – М.: Мир, 1982. – 328 с.
- Кэри П. Применение спектроскопии КР и РКР в биохимии – М.: Мир, 1985. – 272 с.
- Иоффе Б.В., Костиков Р.Р., Разин В.В. Физические методы определения строения органических соединений – М.: Высшая школа, 1984. – 336 с.
- Браун Д., Флойд А., Сейнзбери М. Спектроскопия органических веществ – М.: Мир, 1992. – 300 с.
- Мальцев А.А. Молекулярная спектроскопия – М.: Изд-во МГУ, 1980 – 272 с.
- Накамото К. ИК спектры и спектры КР неорганических и координационных соединений – М.: Мир, 1991 – 536 с.
- Лебедев А.Т. Масс-спектрометрия в органической химии. Издание второе, переработанное и дополненное – Москва: Техносфера, 2015. – 704 с.
- Заикин В.Г., Варламов А.В., Микая А.И., Простаков Н.С. Основы масс-спектрометрии органических соединений – М.: МАИК «Наука/Интерпериодика», 2001. – 286 с.
Матрично-активированная лазерная десорбция / ионизация
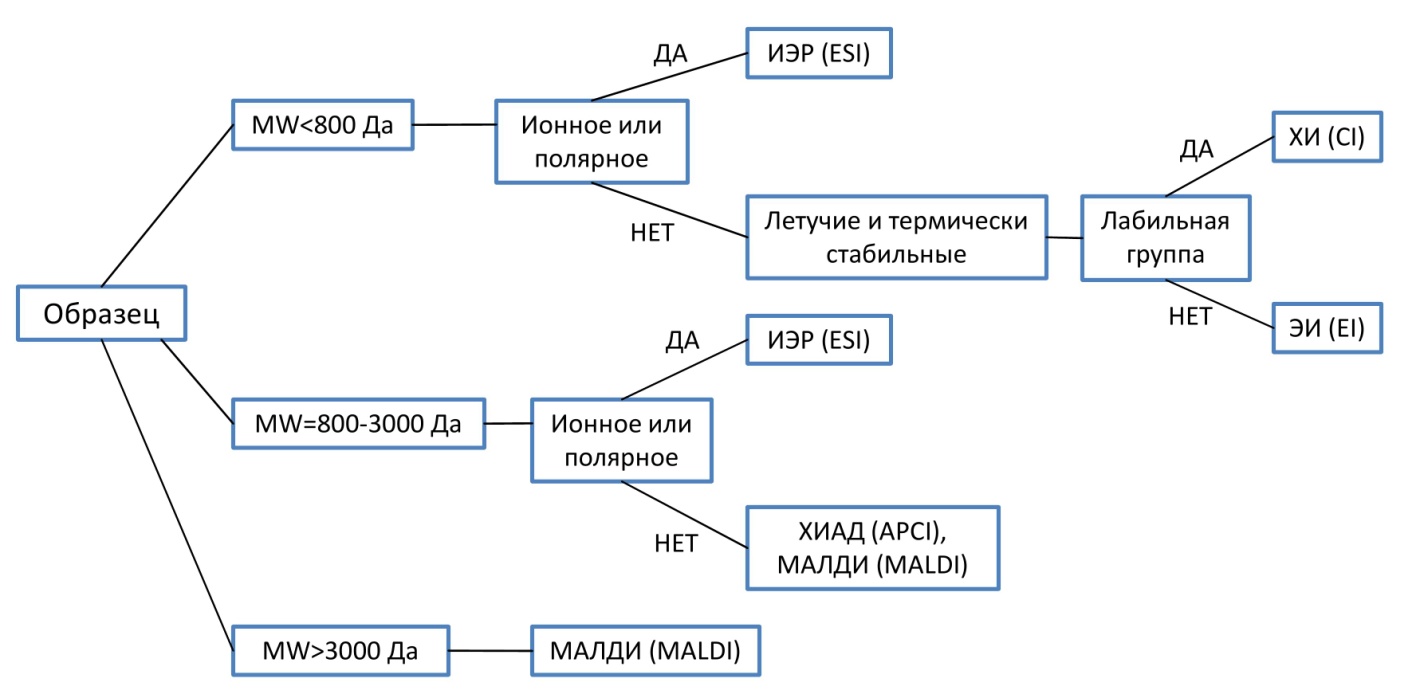
Метод МАЛДИ заключается в облучении короткими лазерными импульсами образца, представляющего собой твердый раствор анализируемого соединения в органической матрице. Над поверхностью образца создается плотная высокотемпературная плазма, в которой наряду с молекулами и ионами матрицы оказываются и молекулы анализируемого соединения. Ионизация последних путем поглощения энергии фотонов или в результате ионно-молекулярных реакций приводит к образованию положительных ([M+H]+, [M+Na]+) и отрицательных ([M-H]—) ионов, которые вытягиваются высоким потенциалом из области ионизации и направляются в анализатор. Метод характеризуется интенсивными пиками молекулярных ионов разного типа и низкой фрагментацией. К настоящему времени методом МАЛДИ успешно анализируются полипептиды, белки, нуклеотиды, полисахариды, синтетические полимеры, гуминовые кислоты, фуллерены, органические комплексные соединения и т. д. Данным методом доступны для анализа термолабильные, труднолетучие, высокомолекулярные соединения.
Оборудование: масс-спектрометр тандемный Ultraflex III TOF/TOF «Bruker», Германия
Химическая ионизация при атмосферном давлении
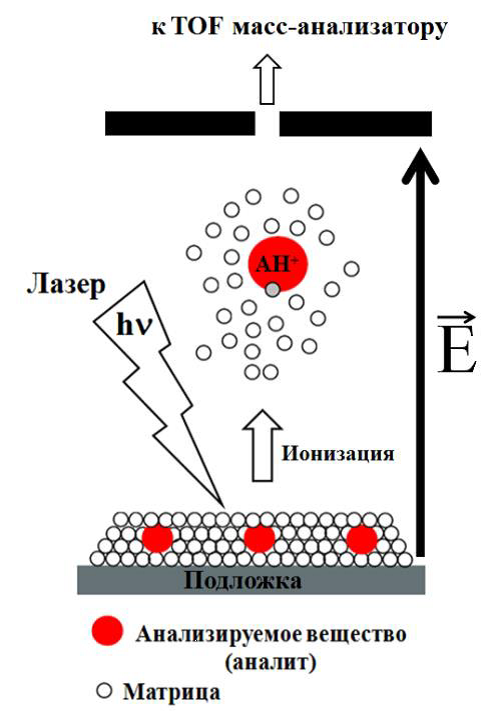
Поток из колонки жидкостного хроматографа направляется в распылитель, где он превращается в мелкодисперсный аэрозоль, смешиваясь с большим количеством нагретого газа (обычно азот или воздух). Капельки аэрозоля в окружении газового потока перемещаются в область испарения, где в газовую фазу переходит большая часть молекул растворителя. Далее на пути потока следует область ионизации. Так как в источнике поддерживается атмосферное давление, ионизация осуществляется за счет коронного разряда. Поскольку количество молекул растворителя существенно превышает количество молекул анализируемого вещества, создаются условия химической ионизации. На выходе из источника ионов расположен ряд последовательных сепараторов с узкими входными отверстиями. Здесь происходит откачка легких молекул для снижения избыточного давления. В результате в анализатор, работающий в условиях глубокого вакуума, поступают в основном ионы анализируемого вещества.
Оборудование: масс-спектрометр AmaZon X «Bruker», Германия
Ионизация электрораспылением
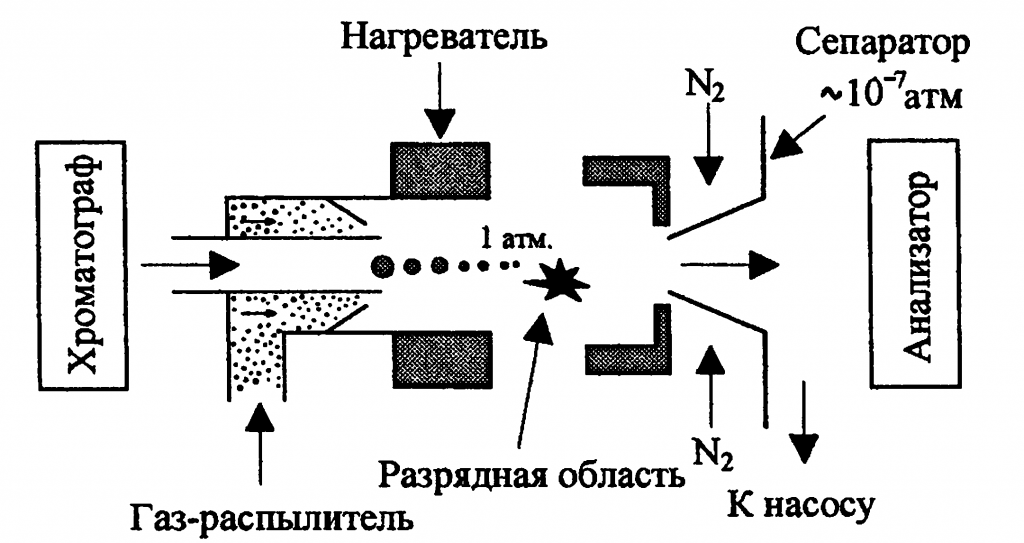
Ионизация электрораспылением относится к «мягким» методам ионизации не разрушающим (как правило) молекулу аналита. Поток из жидкостного хроматографа направляется в иглу диаметром 0,1 мм, на которую подается высокое напряжение порядка 6 кВ. На выходе из иглы в источнике ионов образуется аэрозоль из заряженных капель с высоким поверхностным зарядом. Эти капли движутся к противоэлектроду, имеющему потенциал Земли. В этом же направлении уменьшается и давление, хотя в целом в этой части ионного источника (до противоэлектрода) давление поддерживается на уровне атмосферного. По мере движения к входному отверстию первого сепаратора капли уменьшаются в размере за счет испарения растворителя. Достигая критического размера, при котором силы поверхностного натяжения далее не могут противостоять силам кулоновского отталкивания (предел Релея), капля «взрывается» с образованием более мелких капелек. Этот процесс повторяется. В итоге возникают микрокапли, содержащие всего одну заряженную частицу, которая может оказаться в газовой фазе после испарения остаточных молекул растворителя. Альтернативный механизм предусматривает выброс заряженной молекулы с поверхности одноименно заряженной капли. В обоих случаях в газовой фазе оказываются несольватированные молекулы анализируемого вещества, которые проходят через сепаратор и оказываются в анализаторе.
Особенностью ИЭР является образование многозарядных ионов, что позволяет получать масс-спектры больших молекул.
В качестве подвижной фазы нами обычно используются смеси MeOH/H2O и ACN/H2O. Образцы могут быть проанализированы как в положительном, так и в отрицательном режиме регистрации ионов.
Оборудование: масс-спектрометр AmaZon X «Bruker», Германия
Химическая ионизация
Химическая ионизация (ХИ) является «мягким» методом ионизации, применение которого полезно в тех случаях, когда при ЭИ не наблюдается молекулярного иона. При ХИ молекулы исследуемого вещества в паровой фазе не подвергаются бомбардировке электронами с высокой энергией. Газ-реагент (обычно метан или изобутан) вводится в источник и ионизируется. Молекулы исследуемого вещества сталкиваются с ионизированными молекулами газа-реагента (CH5+, C4H9+ и т.д.) при относительно высоком давлении в камере химической ионизации и подвергаются вторичной ионизации путем переноса протона с образованием ионов [M+1]+, электрофильного присоединения с образованием [M+15]+, [M+29]+, [M+41]+. Фрагментация при ХИ оказывается незначительной, так как избыточная энергия, которая переносится на молекулы образца во время ионизации, мала.
ХИ обычно используется для получения интенсивных пиков молекулярных ионов, протонированных или катионированных молекул.
Оборудование:
– хромато-масс-спектрометр высокого разрешения с двойной фокусировкой DFS «ThermoFisherScientific», США
Электронная ионизация
Электронная ионизация (ЭИ) является классическим методом ионизации в масс-спектрометрии. Молекула вещества пробы в газовой фазе подвергается бомбардировке пучком электронов с высокой энергией (70эВ). Электрон, пролетая вблизи молекулы, возбуждает ее электронную оболочку. Собственные электроны молекулы перемещаются на более высокие орбитали и могут покинуть молекулу, образуя катион-радикал, называемый молекулярным ионом.
Эффективность ионизации очень низка. Фактически ионизируется примерно одна из десяти тысяч молекул образца. Вероятность ионизации меняется от вещества к веществу. В процессе ионизации молекулярный ион получает избыточную внутреннюю энергию в диапазоне 0-20 эВ. Эта избыточная энергия равномерно распределяется по всем связям, причем превышение энергии какой-либо связи, ведет к ее разрыву с отщеплением нейтральной радикальной частицы и образованием четноэлектронного осколочного (фрагментного) иона. Именно поэтому масс-спектры ЭИ имеют сложный вид. В то же время наличие сигналов осколочных ионов дает информацию о структуре молекулы. Этот метод дает возможность идентификации соединений путем сравнения полученного масс-спектра со спектрами из базы данных. Поскольку давление в источнике ионов в условиях ЭИ – 10-5–10-6 мм.рт.ст., а образец можно нагревать до нескольких сотен градусов, в газовую фазу переходят многие органические соединения. Тем не менее, для анализа термолабильных, высокомолекулярных, труднолетучих соединений метод не пригоден.
Анализируемые образцы могут быть в твердом, жидком или газообразном состоянии. Возможен как прямой ввод образца, так и с помощью газового хроматографа.
Оборудование:
– хромато-масс-спектрометр высокого разрешения с двойной фокусировкой DFS «ThermoFisherScientific», США


